UDI mit abacus für Sage 100 umsetzen
Tipps zur Umsetzung der UDI-Anforderungen für Medizinprodukte
Unique Device Identification (UDI) mit abacus realisieren
Die Themen Etikettierung/Produktkennzeichnung und Rückverfolgbarkeit sind nicht neu für uns. Seit mehr als 10 Jahren gibt es schon eine Erweiterung für die Sage 100 um eine lückenlose Rückverfolgbarkeit von Produkten zu gewährleisten. Medizinproduktehersteller wissen, dass auf Basis der Medical Device Regulation (MDR) ein UDI-System verpflichtend ist. Für die USA gibt es von der amerikanischen Gesundheitsbehörde (FDA) bereits länger eine vergleichbare regulatorische Anforderung.
Im folgenden Beitrag werden wir auf diese vier Themenfelder genauer eingehen und einige Empfehlungen zur Einführung geben.
1. UDI Produktdaten – Welche Daten sind für die Kennzeichnung wichtig?
Im ersten Schritt müssen Sie sich darüber im Klaren sein, welche Produktdaten für die Kennzeichnung relevant sind. Im Wesentlichen ist zwischen zwei Produktdatentypen zu unterscheiden. Es gibt auf der einen Seite die statischen Daten (Device Identifier kurz DI) eines Produktes und auf der anderen Seite gibt es dynamische Daten (Production Identifier kurz PI). Die statischen Daten können mit der GTIN (Global Trade Item Number) verglichen werden. Die GTIN dient der eindeutigen Artikelidentifikation und ist weltweit überschneidungsfrei. Zu den dynamischen Daten (UDI-PI) gehören Informationen, wie zum Beispiel das Verfallsdatum, die Charge oder die Seriennummer. Welche dynamischen Daten für ein bestimmtes Medizinprodukt relevant sind, muss die Produktentwicklung eines jeden Unternehmens selbst bestimmen und hängt von verschiedenen Aspekten, wie z. B. der Risikoklasse des Medizinproduktes, ab.
Der große Vorteil der Sage 100/abacus Branchenlösung ist, dass sowohl die statischen (DI) als auch die dynamischen (PI) Daten direkt in der Sage 100 gepflegt werden. Die UDI-DI (nach GSI-Standards, also die GTIN) wird z. B. in den Artikelstammdaten gepflegt, wobei es in der Sage 100 auch möglich ist, für jede Artikelvariante eine eigene GTIN zu vergeben. Die dynamischen Daten (PI) werden im Rahmen der erweiterten Chargenverwaltung von abacus erfasst und ebenfalls in der Sage 100 verwaltet. Im Rahmen einer Produktion kann eine neue Charge oder Seriennummer mit einem bestimmten Verfalls- und/oder Herstelldatum vergeben werden.
Kurz gesagt sind für die Medizinproduktkennzeichnung im wesentlich die GTIN und weitere produktionsspezifischen Informationen, wie z. B. die Chargennummer und das Verfallsdatum wichtig. Im nächsten Schritt geht es dann darum zu bestimmen, wie die Informationen auf das Medizinprodukt gedruckt werden.
2. UDI Datenträger – In welcher Form können die Daten kodiert werden?
Um die relevanten statischen und dynamischen Daten auf ein Medizinprodukt bzw. eine Verpackung aufzubringen, stehen zwei Barcodetypen zur Verfügung, wenn man sich an die Vorgaben der GS1 (einer möglichen zugelassenen Issuing Agency in der EU) hält.
Möglichkeit 1: GS1-128 Strichcode
Wenn man sich auch hier an die Vorgaben der GS1 hält, kann man für die Datenkodierung den GS1-128 Barcode verwenden. Der GS1-128 Barcode ist eher ein klassischer maschinenlesbarer alphanumerischer Strichcode. Diese Art von Strichcode wird zum Beispiel auch für Transportetiketten mit NVE (Nummer der Versandeinheit) verwendet. Für Medizinprodukte bzw. deren Verpackungen ist dieser Strichcode jedoch oft zu groß und nimmt auf der Verpackung zu viel Platz weg. Daher gibt es eine zweite Möglichkeit.
Möglichkeit 2: Data Matrix Code
Die zweite und meist auch gängigere Möglichkeit die Daten zu kodieren, ist die Verwendung eines Data Matrix Codes. Dies ist ein zwei-dimensionaler Code und erinnert leicht an einen QR-Code, er ist jedoch deutlich komplexer. Der Data Matrix Code ist quasi ein wahres Platzwunder, so dass auf sehr kleiner Fläche viele Informationen verschlüsselt werden können.
Klarschrift
Neben dem Barcode müssen die dynamischen und statischen Produktdaten auch noch unmittelbar in der Nähe des Barcodes in Klarschrift und für den Menschen lesbar aufgedruckt werden. Was genau noch „Menschen lesbar“ ist, wird auch von der GS1 beschrieben. Wenn etwas nur mit Hilfe einer Lupe oder eines Mikroskops lesbar ist, gilt es nicht mehr als „für den Menschen lesbar“. Eine normale Brille darf man aber ruhig tragen.
3. UDI Datenbank
Das dritte UDI Themenfeld ist die UDI Datenbank. Für unterschiedliche Regionen gibt es unterschiedlichen Datenbanken, die relevant sind. In der EU wird die EUDAMED-Datenbank mit den statischen Produktdaten zu befüllen sein. Für die USA ist es z. B. die GMDN Datenbank. Start der Datenpflege in der EUDAMED-Datenbank, unabhängig von der Risikoklasse, wird voraussichtlich 2022 sein. Dabei müssen je Produkt etwa 36 – 50 statische Attribute gepflegt werden. Die EUDAMED Datenbank wird mehrsprachig sein und über ein XML-Dateiformat können die Daten ebenfalls hochgeladen werden. In der USA bietet die FDA eine Weboberfläche an um die Information manuell einzupflegen. Oder die Daten werden über ein HL7-SPL Dateiformat zur FDA hochgeladen.
4. Die Basic UDI-DI
Laut Medical Device Coordination Group Document – MDCG 2018-1 v3 ist die Basic UDI-DI folgendes: „The Basic UDI-DI is the main key in the database and relevant documentation (e.g. certificates, declaration of conformity, technical documentation and summary of safety and clinical performance) to connect devices with same intended purpose, risk class and essential design and manufacturing characteristics. It is independent/separate from the packaging/labelling of the device and it does not appear on any trade item.
Any Basic UDI-DI shall identify the devices (group) covered by that Basic UDI-DI in a unique manner.“
Das bedeutet, dass es eine Art Artikelgruppennummer ist, unter dieser Nummer werden ähnliche Artikel („devices with same intended purpose, risk class and essential design and manufacturing characteristics“) gruppiert. Jeder Artikel kann nur zu einer Artikelgruppe gehören und kann auch nur einmal einer Gruppe bzw. einer Basic UDI-DI zugewiesen werden. Die Basis UDI-DI ist in erster Linie für Dokumente, wie z. B. der EU-Konformitätserklärung, die Registrierung in der EUDAMED und für die technische Dokumentation relevant. Sie wird jedoch nicht auf dem Produkt bzw. auf der Verpackung angebracht und muss damit auch nicht in ein maschinenlesbares Format übertragen werden.
Die Basic UDI-DI kann nach der Global Model Number aufgebaut werden. Das bedeutet, dass sie aus der GS1 Basisnummer, der fortlaufenden Artikelgruppennummer (z. B. 001-999) und einer Prüfziffer besteht.
Checkliste zur Einführung von UDI
Das UDI-Projekt ist kein einfaches "Etikettierungsprojekt“ und bedarf einer guten Planung mit entsprechendem Konzept. Die Punkte der Checkliste geben einen ersten Anhaltspunkt, damit an die wesentlichen Aspekte gedacht wird.
Download der Checkliste Einführung UDI
Für die erfolgreiche Umsetzung sollten alle Prozessschritte und Themenfelder rund um die Kennzeichnung der Medizinprodukte berücksichtigt werden. Wichtig sind zum Beispiel Artikelstammdaten, Chargenverwaltung, das Produktdesign, der Druckprozess usw.. Erstellen Sie also im ersten Schritt zum Beispiel eine Mindmap, um alle Themen rund um die Kennzeichnung zu erfassen. Sie werden feststellen, dass viele Bereiche und entsprechende Mitarbeiter Ihres Unternehmens mit involviert werden sollten.
Pflegen Sie Ihre Stammdaten
Ein gutes Stammdatenmanagement ist gar nicht so einfach im Unternehmen ganzheitlich umzusetzen, wie man denkt. Beim ersten Anlegen der Artikelstammdaten ist der Prozess in vielen Unternehmen noch relativ klar definiert, aber das ist nicht alles. Die Frage ist dann, was muss beachtet werden, wenn sich z. B. etwas an der Verpackung verändert oder wenn der Produktname sich nochmals ändert. Deshalb ist es wichtig, dass es auch einen klaren Prozess für die Änderung von Stammdaten geben sollte. Korrekte und vollständige Stammdaten sind das A und O im Rahmen eines UDI-Projekts.
Nutzen Sie eine professionelle Chargenverwaltung
Wie zu Beginn der Beitrags beschrieben, sind für die Kennzeichnung zwei Produktdatentypen relevant. Es gibt auf der einen Seite die statische Daten (Device Identifier kurz DI) eines Produktes und auf der anderen Seite gibt es dynamische Daten (Production Identifier kurz PI). Die statischen Daten sollten in den Artikelstammdaten gepflegt werden. Die dynamischen Daten eines Produktes, die mit der Produktion in Verbindung stehen, werden in der Regel jedoch in einer Chargenverwaltung gepflegt. Im Rahmen der Sage 100 wäre das die erweiterte Chargenverwaltung von abacus (nähere Infos dazu finden Sie hier). Dort werden die Produkte und je Charge Informationen, wie zum Beispiel das Verfalls- und Herstelldatum, die Charge oder die Seriennummer erfasst. Nur so ist es möglich, dass alle relevanten Daten in einem integrierten System enthalten sind und im Rahmen des Etikettendesigns und -drucks auf diese Daten zugegriffen werden kann.
Weitere Quellen:
Wenn Sie weitere Informationen rund um UDI, MDR und EUDAMED suchen, können wir folgende Internetseiten empfehlen:
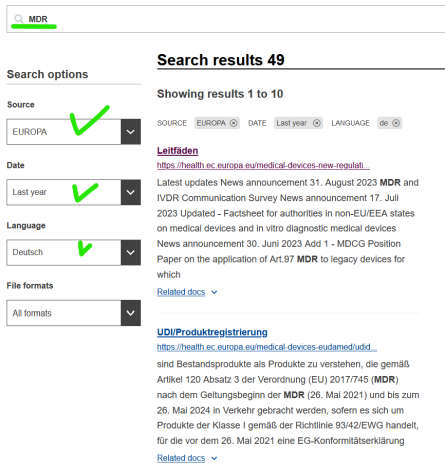
- Dokumente zu MDR/IVDR (Medizinprodukteverordnung) der EU Kommission: Medical Devices - New regulations EU Commission
- Informationen zu UDI der EU Kommission: Search "UDI" in European Commission Database
- Leitlinie der UDI-Working-Group zum Thema Basic UDI-DI und UDI-DI Eigenschaften
- Das Johner Institut bietet eine Reihe an Informationen rund um UDI
- GS1-Germany als Zuteilungsstelle bietet ebenfalls viel Informationen zu dem Thema an
Wenn Sie sich für ein UDI-Projekt, Etikettierung oder erweiterte Chargenverwaltung für Sage 100 interessieren, können Sie uns natürlich gerne kontaktieren.